Guía Práctica del laboratorio microbiológico en agua y alimentos (Parte XIV)
"Lo poco que hoy soy, lo soy en razón de todo lo que he aprendido"
(El Autor)
GUÍA PRACTICA del LABORATORIO MICROBIOLOGICO
en AGUA y ALIMENTOS (Parte XIV)
b. ALIMENTOS
Hay una serie de razones que justifican la necesidad
de analizar los alimentos para determinar cualitativa o cuantitativamente sus
microorganismos. los principales objetivos
del análisis microbiológico son asegurar:
(1) que el alimento cumple ciertas normas
estatutarias;
(2) que se ajusta a normas internas establecidas por
la compañía procesadora y a las externas exigidas por el
comprador;
(3) que las materias alimenticias que llegan a la
factoría para ser procesadas cumplen las normas exigidas y las pactadas con el
productor;
(4) que se mantienen el control del proceso y la
higiene de la línea de fabricación.
Los métodos del examen microbiológico utilizados
para controlar la calidad del alimento son en sí mismos muy variados y
dependientes, en gran parte, del alimento que va a ser analizado. Conviene
estudiar los análisis bajo los siguientes encabezamientos:
1. Estimación del número total de microorganismos.
2. Estimación del número de microorganismos
indicadores.
3. Examen o estimación del número de
microorganismos alterantes de los alimentos y de otros grupos especiales.
4. Examen o estimación del número de
microorganismos productores de toxiinfecciones alimentarias y de los
microorganismos patógenos transportados por los alimentos.
5. Análisis de los productos metabólicos de
los microorganismos; a menudo requieren técnicas más sofisticadas de las que
sólo disponen los laboratorios mejor dotados.

Uno de los mayores problemas del análisis
microbiológico de los alimentos es determinar el número de muestras de un lote
o de un día de trabajo que deben analizarse para asegurar que el producto o
material alimenticio cumple la norma exigida. Obviamente cuanto mayor sea el número de muestras tomadas, mayor será la
confianza en los resultados, pero puesto que el alimento empleado con fines
analíticos representa un gasto no recuperable, debe alcanzarse un compromiso
entre la exactitud de los resultados y la economía del análisis. los esquemas
de muestreo, actualmente en uso, implican el análisis de cinco o diez muestras
por lote, o de la raíz cuadrada del número de envases por lote; sin embargo,
podría argüirse que una cantidad tan grande de muestras está totalmente
injustificada cuando se obtienen resultados concordantes buenos.

Por lo
tanto, las fuentes microbianas disponibles deben usarse prudentemente y el
muestreo será máximo con los alimentos que se sabe que son microbiológicamente
peligrosos y con los que dan resultados erráticos; el muestreo será también
grande con los que se han sometido a un cambio de procesado y siempre que haya
tenido lugar un fallo en la línea de procesado. También debe tenerse en cuenta
que el número de análisis se ve afectado por la razón o causa que lo motiva;
así, se necesitan menos pruebas para la confirmación de un estándar o norma
satisfactorio que cuando el fin perseguido es la eliminación de un producto no
satisfactorio. Cualquier esquema de
muestreo digno debe tener una base estadística y a los lectores que necesiten
mayor información sobre tales esquemas les recomiendo la lectura de
Microorganismos de los alimentos, Vol. 2 (Comisión Internacional de
Especificaciones Microbiológicas para los Alimentos, ICMSF, 1974* - *Esta obra
ha sido publicada en español por EDITORIAL ACRIBIA, S. A., Zaragoza) en donde
encontrarán todos los datos que precisen. La Comisión
Internacional (ICMSF), citada en el punto anterior, define a la “muestra
representativa” como aquélla cuyo estado es tan parecido como sea posible a la
del lote (o partida) del que se tomó. Por lo tanto, es necesario evitar todo
tipo de perjuicio y asegurarse de que se toman suficientes muestras. Como mejor
se realiza esto es mediante el muestreo al azar, utilizando tablas de números
aleatorios según recomienda la Comisión (ICMSF, 1974). Sin embargo, debe
tenerse en cuenta el posible aumento de microorganismos en el equipo y por lo
tanto en el alimento, durante la producción de una partida; el producto suele
contener muchos menos microorganismos al comienzo que a la terminación del
trabajo de la fábrica, lo que deberá tenerse presente en cualquier esquema de
muestreo. De otra parte, si el equipo
se ha limpiado mal, los alimentos pueden contaminarse mucho al iniciarse el
trabajo. En consecuencia, puede ser ventajoso retirar los productos a
intervalos de tiempo regulares; ello no supone una depreciación del muestreo al
azar y se emplea frecuentemente.

Otras dificultades del muestreo
derivan de la consistencia heterogénea del producto alimenticio y si el
alimento no es homogéneo se requiere un muestreo más frecuente. Como ejemplos
extremos se pueden citar la leche, de la que sólo se requiere una pequeña
muestra del alimento bien mezclado y algunos de los productos actuales,
compuestos de múltiples ingredientes, lo que puede hacer imposible obtener la
cantidad requerida de cada uno para contar con una muestra representativa;
consecuentemente debe hacerse un análisis por separado de cada
componente. Cuando los microorganismos
se limitan a zonas específicas del alimento el muestreo es en ocasiones
deliberadamente desequilibrado, por ejemplo, en alimentos como la carne, el
pescado y la fruta la mayoría de sus microorganismos se localizan en las
superficies externas y son éstas, por lo tanto, las que constituyen las
principales regiones de muestreo. Los alimentos líquidos no presentan
problemas y corrientemente se muestrean con pipetas después de mezclarse bien.
Los alimentos sólidos los presentan a menudo, por lo que para superar las
dificultades de la toma de muestras se utilizan diversas técnicas.

En alimentos
cuyas unidades son relativamente manejables, como aves y pescado, la canal
entera se lava con agitación en un medio de muestreo líquido, si bien se admite
que con tal tratamiento sólo se recupera una parte de la flora; se obtienen
recuentos mayores si se incluyen en la solución de lavado abrasivos, como arena
estéril. Durante muchos años se han usado mucho para el muestreo de superficies
las torundas de algodón húmedo, pues tienen la ventaja de ser de fácil manejo y
cuando se utilizan conjuntamente con una lámina metálica, dotada de ventana,
permiten la toma de muestra de un área superficial equivalente; después de
frotada dicha área, el soporte de la torunda se rompe y aquélla se separa y
deja caer en un diluyente agitándose entonces para separar los microorganismos
del algodón. Las recuperaciones alcanzadas con estas técnicas de la torunda son
pobres, debido a la adherencia de los microorganismos a la superficie del
alimento y a su retención en la torunda, pero pueden mejorarse, si al área
muestreada vuelve a frotarse con otra torunda seca. los métodos del agar de
contacto, en los que un medio estéril sólido a base de agar se presiona contra
la superficie a muestrear, dan recuentos todavía menores que los de las
técnicas de la torunda, pero constituyen el sistema de muestreo de uso más
sencillo ya que el medio puede someterse a incubación directamente. En el caso de carnes, pescados y aves, los recuentos más altos se
obtienen con el llamado «muestreo destructivo». Pueden tomarse muestras con
sacabocados pre esterilizados, lo que tiene la ventaja de que se analiza un
área superficial conocida que varía con el diámetro del sacabocados utilizado.
Escalpelos y cuchillas también son bastante populares, pero con tales
instrumentos la relación área superficial/volumen es imposible de controlar.
También
pueden tomarse muestras de áreas conocidas empleando un escarificador dérmico y
un cilindro metálico estéril que contiene el diluyente (Barnes et al., 1973).
Las carnes picadas y los alimentos graniformes, como guisantes y harina, son
más fáciles de muestrear ya que pueden tomarse pesos conocidos. Algunas de las
técnicas de muestreo microbiano estudiadas más atrás sirven también para el
examen del equipo de procesado de los alimentos, por ej., el lavado con un
volumen conocido de agua o de diluyente, el empleo de torundas, posiblemente
con lámina metálica y los métodos del agar de contacto. Excepto cuando se
emplean torundas o lavados, se toma un peso conocido de la muestra del alimento
(por ej., 10 ó 25 g). El alimento se adiciona a un diluyente estéril adecuado,
como solución de Ringer diluida al 1/4 o agua de peptona al 0,1 % y se trata a
continuación de forma que se liberen en el diluyente los microorganismos del
alimento.
El tratamiento implica un mezclado mecánico o un pase por el
Stomacher. En esta última técnica, muy popular actualmente, la muestra, junto
con un volumen conocido de diluyente, se coloca en una bolsa de plástico
estéril que es golpeada por una especie de paletas en el interior del
Stomacher. El volumen de diluyente utilizado generalmente es nueve veces mayor
que la muestra (por ej., 25 g de guisantes en 225 ml de diluyente) de forma que
se obtenga un homogeneizado 10-1, a partir del cual se preparan las
correspondientes diluciones (10-2, 10-3, 10-4,
etc.) dependiendo de la calidad microbiológica del alimento o superficie objeto
del análisis. Una de las pruebas microbiológicas más corrientes llevadas a
cabo en los alimentos es el recuento viable total, conocido también como
recuento estándar en placa y recuento aeróbico en placa. Para ello se siembran
diluciones adecuadas de una muestra de los alimentos en medios de agar que
contienen nutrientes suficientes para permitir el crecimiento del mayor número
posible de microorganismos. los nutrientes de que se compone, por ejemplo el
agar nutritivo, (Nutritive Agar, Oxoid) son: extracto de carne, extracto de
levadura y peptona (un hidrolizado enzimático de carne fresca que contiene
diversas sales inorgánicas, factores de crecimiento y péptidos). El pH del medio
se ajusta generalmente a 7 – 7,4 para recuperar las bacterias y no los mohos y
levaduras.
Las células bacterianas individuales, transferidas a la placa con el
diluyente, se multiplican normalmente durante la incubación. Así puede hacerse
una estimación del número total de células viables (es decir, células capaces de
crecer en el medio de recuperación) en la dilución sembrada, calculando después
de la incubación el recuento del número total de colonias bacterianas que se
desarrollan; naturalmente en las condiciones aerobias normales crecerán las
aerobias obligadas y las aerobias facultativas. Para estar seguro de que el cultivo es puro, repetir el proceso entero;
para ello tomar una colonia aislada y sembrar por estrías una segunda
placa. Las temperaturas de incubación seleccionadas dependen del alimento
que va a examinarse. Las temperaturas corrientemente utilizadas son 45º C para
las termófilas, 37º C para las mesófilas y 20º C para mohos y levaduras.
Mientras la última temperatura es conveniente para las bacterias psicrótrofas y
también para muchas mesófilas, para una estimación más exacta de las
psicrótrofas se utilizan a veces temperaturas más bajas (por ej., 1 – 7º C);
debe recordarse siempre que ninguna temperatura de incubación excluye por
completo a todos los microorganismos de otro grupo. Son
muchas las técnicas en placa empleadas para la enumeración del número total de
bacterias viables, de las que describiremos brevemente cinco. La enumeración de
las colonias se lleva a cabo tradicionalmente de forma manual, con el empleo de
un contador de colonias iluminado, con cuya ayuda el laborante cuenta cada
colonia individual (véase más abajo). Esta operación puede ser tediosa e
inexacta, salvo que en el medio de cultivo haya crecido un número adecuado de
colonias (idealmente menos de 300, si bien por razones estadísticas se
requieren también como mínimo 30 colonias). En los últimos años se han ideado
una serie de instrumentos de recuento automático de colonias que permiten
obtener en pocos segundos recuentos exactos.
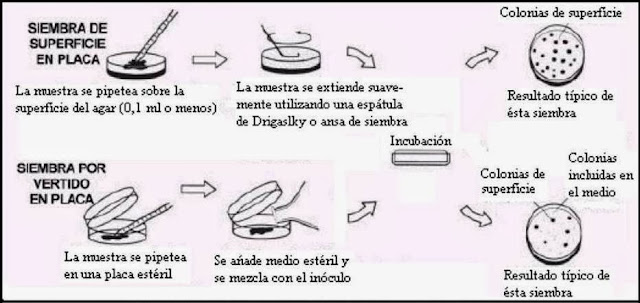
En el método de vertido en
placa, se vierten en una serie (o mejor dos series) de placas de
Petri alícuotas de 1 ml de las diluciones apropiadas del alimento. A
continuación se adicionan a cada placa unos 10 – 15 ml de agar nutritivo
fundido, enfriado a 45º C, y se mezcla cuidadosamente con la alícuota
correspondiente. Después de solidificado el agar, se incuban las placas a la
temperatura requerida durante un tiempo que depende de las condiciones de
incubación (por ej., 1 – 2 días a 37º C, 3 – 4 días a 20º C y 7 – 10 días a 5º
C). Después de la incubación se contarán las
colonias de las placas que contienen entre 30 y 300 colonias; a partir de este
recuento puede calcularse fácilmente el número de bacterias viables por gramo
(o por cm2) de alimento. En el método de
extensión en placa, se vierte previamente el medio en placas de Petri y se deja
solidificar; a continuación se extienden uniformemente por la
superficie alícuotas de 0,1 ml de las correspondientes
diluciones mediante el empleo de varillas de vidrio estériles en forma de L
(Espátula de Drigalsky).
Las placas se incuban como
antes. Las ventajas de esta técnica son: primero que las células bacterianas
termosensibles (esto es las psicrótrofas) no se destruyen por el agar fundido,
lo que podría ocurrir, en cierta extensión con el método anterior, si la
temperatura del agar es demasiado alta; segundo, todas las colonias crecen en
la superficie del agar y pueden observarse y picarse fácilmente si fuera
necesario, mientras que en el método de vertido en placa muchas colonias se
desarrollan incrustadas en el agar, teniendo menor tamaño y siendo más difíciles
de subcultivar. Con esta técnica de la gota en placa, también se emplea un
medio de agar solidificado. Se utilizan pipetas especialmente calibradas que
vierten 0,02 ml por gota. En la superficie de la placa se dejan caer cinco
gotas separadas (o sea 0,1 ml) que se dejan secar antes de la incubación. Sólo
deben contarse las placas cuyas diluciones producen 20
colonias por gota. Puesto que los métodos citados además de requerir
bastante tiempo son caros en material, se ha desarrollado otro más rápido que
utiliza menores cantidades, es el método de la «gotita de agar». En esta
técnica las diluciones se preparan con agar fundido y las colonias se
desarrollan en las gotas solidificadas (0,1 ml) durante la incubación. El
recuento de las colonias se facilita empleando un visor de proyección que
amplía las gotitas unas diez veces aproximadamente. Otro método semiautomático, cada vez más popular, es el de la placa en
espiral, en el que una máquina vierte continuamente un volumen conocido de
muestra en la superficie de una placa de agar que gira. La cantidad de muestra
depositada disminuye a medida que el tubito dosificador se desplaza desde el
centro a la periferia de la placa girante; de esta forma durante la incubación
las colonias bacterianas se desarrollan siguiendo un trazo en espiral.
El
recuento puede realizarse manualmente empleando una red de contaje o mediante
contadores de colonias basados en rayos láser, especialmente diseñados para su
empleo con esta técnica. Comparaciones realizadas con métodos más tradicionales
han demostrado que no hay diferencias significativas en los recuentos
obtenidos. A medida que los microorganismos se multiplican en
un medio de crecimiento, acaecen diminutos cambios de impedancia que pueden
medirse haciendo pasar por el medio una pequeña corriente eléctrica. A una concentración concreta de microorganismos tiene lugar un cambio
marcado de impedancia y como es lógico, con una carga bacteriana inicial más
alta esta concentración umbral se alcanza antes. Así puede estimarse el
número de microorganismos inicialmente presentes en el alimento; para ello se
registra el tiempo requerido (tiempo de detección) para alcanzar el umbral,
empleando muestras del alimento diluidas en un medio de crecimiento. Se ha
demostrado que hay una buena concordancia entre los recuentos viables
convencionales y los tiempos de detección. Además, los tiempos requeridos para
los análisis son normalmente de unas 5 horas lo que permite estimar rápidamente
la calidad. En ocasiones puede necesitarse obtener el número
total de microorganismos (esto es, células viables y muertas) de nuestros
alimentos como, por ejemplo, alimentos enlatados y leche pasteurizada. En
portaobjetos de vidrio se hacen extensiones de la muestra, generalmente
diluida, que se tiñen con un colorante adecuado. Se cuenta el número total de
células microbianas de un número dado de campos microscópicos y del recuento
obtenido puede calcularse aproximadamente el número total de microorganismos
por gramo de alimento.
El análisis rutinario de los alimentos para poner de
manifiesto un amplio rango de bacterias patógenas es impracticable en la
mayoría de los laboratorios, bien porque están inadecuadamente
dotados, bien porque el tamaño de la muestra impediría su
manejo convenientemente. Por ello se ha convertido en práctica corriente
investigar en los alimentos la existencia de bacterias que indican la posibilidad
de la presencia de las productoras de toxiinfecciones alimentarias o de otras
patógenas. Por ello se les denomina
«microorganismos indicadores» y se catalogan frecuentemente como de gran
importancia al establecer la seguridad y calidad microbiológica de los alimentos.
Las principales bacterias empleadas como indicadores son coliformes,
enterococos y, más recientemente, enterobacteriáceas. En ocasiones resultan una
buena guía los recuentos viables totales a 37º C, si bien su relación con la
seguridad de los alimentos es más bien débil. Una vez que se
obtiene un cultivo puro, normalmente se ha de propagar (se le hace crecer de
nuevo). Seguramente, el investigador deseará obtener más células para poder
trabajar con ellas. Para cultivar microorganismos en el laboratorio, se ha de
preparar un medio de cultivo, líquido o sólido, con todos los nutrientes
necesarios para su crecimiento. Los medios sólidos se hacen generalmente,
añadiendo agar a los líquidos. El tipo de
medio que utiliza un microbiólogo depende del microorganismo que está
cultivando y el porqué de dicho cultivo. Los microorganismos presentan una
enorme variedad de requerimientos nutricionales. Se
utiliza un medio mínimo para determinar los requerimientos nutricionales de un
organismo y un medio rico si se desea obtener masa celular de una forma rápida.
Los medios se pueden formular para el desarrollo de una especie o para
distinguir entre especies o cepas. Por tanto, los medios se clasifican en
definidos, complejos o indefinidos, selectivos, diferenciales, selectivos –
diferenciales y de enriquecimiento, dependiendo de su composición y uso. Un
medio definido es aquel del cual conocemos su composición química exacta,
porque ha sido preparado a partir de compuestos químicos
puros. Escherichia coli es capaz de crecer en un medio
químicamente definido, de composición bastante sencilla. Este
microorganismo requiere una fuente de carbono orgánica (por ejemplo, glucosa),
pero puede obtener el resto de los nutrientes esenciales a partir de sales
minerales.
En cambio, otros organismos, denominados exigentes, requieren medios
químicamente muy complejos. Por ejemplo, la bacteria Leuconostoc
citrovorum es extraordinariamente exigente ya que requiere un medio con
muchos ingredientes. Los medios definidos se usan generalmente para realizar
estudios genéticos, pero sus inconvenientes a menudo sobrepasan sus ventajas.
Así, se requiere un tiempo considerable para preparar un medio definido y las
bacterias crecen más despacio en ellos. Además, no conocemos los requerimientos
nutricionales de todas las bacterias y, por tanto, no siempre pueden
utilizarse. Los medios complejos, se preparan a partir de extractos de
productos naturales tales como carne, sangre, caseína (la proteína de la
leche), levaduras o soja. Un medio líquido complejo se denomina caldo. La
caseína u otras proteínas que se añaden a los medios son usualmente
hidrolizadas con enzimas o en medio ácido, para hacerlas más solubles y, por
tanto, más fáciles de utilizar nutricionalmente. Una hidrólisis parcial rompe
las proteínas en péptidos. Una hidrólisis total las degrada hasta aminoácidos.
A las proteínas parcialmente hidrolizadas se les denomina peptonas. Entre las
peptonas comerciales se encuentra la proteosa – peptona, la triptona y la
triptosa. A la caseína totalmente hidrolizada se le denomina hidrolizado
de caseína. Los diversos componentes de
un medio complejo se venden como polvos deshidratados. También existen ya
cientos de mezclas complejas que se comercializan como medios complejos
específicos. Uno de estos medios es el caldo nutritivo, probablemente el
medio complejo que más se utiliza. Cuando este medio se solidifica
con agar, se denomina agar nutritivo. Generalmente se prefiere
la utilización de los medios complejos, ya que son fáciles de
preparar y permiten un crecimiento rápido de los microorganismos. Un medio
selectivo favorece el crecimiento de ciertos microorganismos,
mientras suprime el crecimiento de otros. Los medios selectivos se
utilizan para aislar especies particulares a partir de una mezcla compleja. Por
ejemplo, se utiliza un medio selectivo, para aislar Salmonella
typhi, agente causal de la fiebre tifoidea, a partir de heces donde
existen cientos de microorganismos diferentes. Algunos medios son
selectivos porque contienen un producto químico, como la azida sódica, el
telurito potásico o el cristal violeta, que inhiben el desarrollo de
algunos microorganismos pero no de otros.
El agar SPS (denominado de esta forma
porque contiene sulfadiazina y sulfato de polimixina) se utiliza para
identificar Clostridium botulinum, agente causal de una grave
intoxicación alimentaria. El medio SPS permite el crecimiento de esta bacteria,
pero inhibe el de otras especies de Clostridium. otros medios de cultivo
selectivos utilizan un valor extremo de pH o una fuente de carbono
poco común. Los medios diferenciales se utilizan para
identificar las colonias de un determinado microorganismo. Por ejemplo, para
identificar Streptococcus pyogenes, la bacteria que causa la
escarlatina, se utiliza el medio de agar sangre es un agar que contiene
hematíes. Las colonias de esta bacteria muestran a su alrededor una zona
transparente debido a que producen hemólisis (muerte y lisis de los
hematíes). Escherichia coli y las bacterias relacionadas con
ella se identifican en medios con un indicador de pH porque originan productos
metabólicos ácidos, que cambian el color del indicador y por tanto de sus
colonias. Algunos medios son selectivos y diferenciales al mismo tiempo. El
agar MacConkey es un ejemplo de medio selectivo – diferencial, utilizado para
detectar cepas de Salmonella y Shigella, bacterias
entéricas (del intestino) que causan disenterías. Cualquier muestra de heces
enviada al laboratorio esta plagada de bacterias pertenecientes a muchas
especies. El agente selectivo del MacConkey actúa como una especie de tamiz
grosero que disminuye el campo de identificación. El cristal violeta y las
sales del medio inhiben el crecimiento de la mayoría de las bacterias
Gram positivas (Salmonella y Shigella son Gram
negativas). A partir de aquí, el componente diferencial del medio, en este
caso la lactosa, comienza a ser
importante. Salmonella y Shigella no fermentan la lactosa,
pero la mayor parte de las enterobacterias sí lo hacen. Por
tanto, las colonias de estas dos bacterias serán rojas, mientras que las
restantes no lo serán. Un medio de cultivo se
formula para suministrar todos los nutrientes que un microorganismo necesita
para crecer, pero esto no es suficiente. En el laboratorio, también es
preciso aportar las condiciones ambientales adecuadas. Tanto la
temperatura como el pH deben estar dentro del intervalo apropiado; con respecto
al oxígeno, según el caso, será aportado o eliminado. En la
rutina diaria del trabajo de microbiología de agua y alimentos, y reglamentadas
por los principales Organismos de Control Internacionales (CODEX ALIMENTARIUS,
ICMSF, AOAC) y Nacionales (CÓDIGO ALIMENTARIO ARGENTINO), se llevan a cabo las
siguientes marchas de investigación y aislamiento de patógenos, de acuerdo a lo
legislado como “Criterios Microbiológicos” para cada alimento en particular y
que serán descriptas e ilustradas en los blogs que se renovarán a continuación.

"SOMOS LO QUE HACEMOS REPETIDAMENTE. EXCELENCIA, POR LO TANTO, NO ES UN ACTO SINO UN HÁBITO"
ARISTOTELES
LEGALES: El autor no asume responsabilidad alguna por la descarga, copia, distribución, modificación o alteración de los contenidos publicados, sean propios del mismo o de terceros, los cuales pudieren estar protegidos por Copyright, Derechos de Propiedad Intelectual, Derechos de Autor, o relacionados. La Bibliografía del tema expuesto y el crédito fotográfico está en poder del Autor y no se publica dada su extensión, pero se enviará por mail al interesado que la solicitare debidamente fundamentada.


Muchas personas pensarán que las matemáticas solo se usan en el colegio o la universidad http://bibliotheque-du-capucin.com/
ResponderBorrar