NUEVA GUÍA PRÁCTICA del LABORATORIO MICROBIOLÓGICO de AGUAS y ALIMENTOS (XVI Parte)
“El médico del futuro no tratará el cuerpo humano con medicamentos, más bien curará y prevendrá las enfermedades con la nutrición"
(Thomas Alva Edison)
NUEVA GUÍA PRÁCTICA del LABORATORIO MICROBIOLOGICO
de AGUA y ALIMENTOS (XVI Parte)

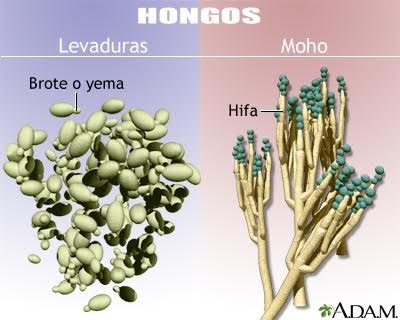
Mohos
y Levaduras
Las
levaduras y los mohos, constituyentes de la flora micótica total a investigar,
generalmente se han cultivado en medios de pH bajo (3,5 - 5,5) y a temperaturas
de 20° - 30º C si bien muchas bacterias crecen en estas condiciones. Para
inhibir las bacterias se utilizan antibióticos de «amplio espectro» que
incorporados a los medios de cultivo inhiben el crecimiento de aquéllas. Un
medio típico es el agar oxitetraciclina-glucosa-extracto de levadura, que lleva
como agente selectivo oxitetraciclina y entre otros nutrientes glucosa y que se
ajusta a un pH relativamente alto, aproximadamente 6,5. Los
métodos de ensayo de las aflatoxinas difieren algo, dependiendo del alimento.
Generalmente el alimento se pica suficientemente y a continuación se extrae con
un solvente adecuado, como el cloroformo. Se purifica el extracto y la fase
siguiente de detección implica algún tipo de cromatografía, generalmente en
capa fina. Con el empleo de solventes que separan netamente las toxinas, se
pueden comparar cualquier tipo de manchas que den fluorescencia bajo la luz UV
con los correspondientes estándares. El significado de la contaminación fúngica de los
alimentos, especialmente por mohos, viene no sólo del potencial de los mohos
para deteriorar los alimentos, sino también del potencial de muchos de ellos
para producir una gran variedad de micotoxinas a las que el hombre es sensible,
así como su capacidad para provocar infecciones e incluso, reacciones alérgicas
a personas hipersensibles a los antígenos fúngicos. En cuanto al significado
para la salud del consumidor, la acción de las levaduras es meramente
infectiva.
De
todo esto se deduce que existe un riesgo potencial en la contaminación fúngica
de los alimentos y, por ello, para conocer la calidad microbiológica de
diversos productos, se procede a la evaluación de su tasa de contaminación por
mohos y levaduras. Después del recuento se puede realizar una
identificación aproximada de las colonias de levaduras y mohos que aparecen en
la placa. La identificación de las levaduras conlleva una serie de pruebas
fisiológicas y bioquímicas, por lo que la metodología en este punto se
aproxima, en cierta medida, a los sistemas clásicos de identificación
bacteriana. Las
técnicas de identificación de mohos se encaminan, casi exclusivamente, al
estudio de la morfología, tanto macroscópica como microscópica: crecimiento,
aspecto de las colonias, características de las hifas, formación de exudado,
pigmentos, micelio, esporas, etc.
Procedimiento:
La siembra de las placas de recuento se lleva a cabo en masa. A partir de la
serie de diluciones decimales se añade 1 ml de la dilución 1/10 y 1/100 en
sendas placas de Petri vacías en las que se añade medio Rosa de Bengala con
cloranfenicol (20 ml/placa aproximadamente) atemperado a 45 - 47ºC. Las placas
se incuban, SIN INVERTIRLAS, a 24ºC durante 4 - 5 días. El recuento se realiza
en la placa que presente un crecimiento entre 0 - 50 colonias. El
crecimiento de mohos y levaduras se caracteriza por el aspecto algodonoso y
cremoso de sus colonias, respectivamente. Para la identificación de
mohos se coge un trozo periférico de una colonia y se homogeneiza en un porta
sobre el que previamente se ha añadido una gota de lactofenol. Se protege la
preparación con un cubre evitando que queden burbujas de aire. Se le añade una
gota de aceite de inmersión y se observan al microscopio las esporas, los
cuerpos fructíferos, el micelio, etc.


Clostridios
Sulfito – Reductores
Contrariamente
a lo que sucede con las salmonelas el aislamiento de un pequeño número de C.
perfringens a partir de los alimentos no significa necesariamente que exista
peligro de toxiinfección alimentaria; sólo cuando hay un gran número existe
verdadero peligro, por lo que con este microorganismo las técnicas de recuento
son imprescindibles. Se emplean las siembras (en placa, por vertido o «en
superficie») de diluciones de homogeneizados del alimento, junto con medios
selectivos. Se han desarrollado muchos de estos medios para C. perfringens: la
mayoría a base de agar, al que se incorporan los nutrientes más convenientes,
sistemas indicadores y agentes selectivos. La
ICMSF ha estudiado comparativamente los métodos de enumeración de C.
perfringens de los alimentos y ha concluido que el agar sulfito-cicloserina
proporciona las mayores recuperaciones de esta bacteria, además del número más
bajo de falsos positivos. Este medio contiene
cicloserina, un antibiótico, y además un sistema indicador que se basa en que
C. perfringens, como otros muchos clostridios, reduce el sulfito o sulfuro,
dando colonias negras en presencia de una sal de hierro.
Después
de la incubación de las placas en anaerobiosis a 37 ºC durante 24 horas, las
colonias sospechosas se inoculan en un medio confirmativo, observando la
movilidad (C. perfringens es inmóvil) y la capacidad de reducir los nitratos a
nitritos. Otra prueba confirmatoria consiste en
sembrar las colonias sospechosas en placas de agar yema de huevo, a una de
cuyas mitades se le añade antitoxina de C. perfringens. Después de la
incubación las colonias crecidas en la mitad de la placa carente de antitoxina,
están rodeadas de una zona opaca (reacción de Nagler), mientras que las de la otra
mitad no muestran cambios ya que la reacción ha sido específicamente
neutralizada por la antitoxina. C.
botulinum corrientemente no se enumera en los alimentos y las pruebas que con
él se emplean implican generalmente la detección de toxinas botulínicas en el
alimento y el aislamiento de C. botulinum, seguido de la detección de sus
toxinas. Debe tenerse un cuidado extremo al analizar los alimentos sospechosos
y es necesario el consejo de un experto antes de embarcarse en tales
análisis. Si se dispone de buen laboratorio los homogeneizados de alimentos se
pueden examinar directamente al microscopio poniendo de manifiesto la presencia
de células enteras y de esporas con ayuda de las técnicas de tinción
fluorescente. También deben sembrarse en estría muestras de alimentos en agar
sangre, preferiblemente con yema de huevo para que se obtenga después de una
incubación de 3 días a 30º C en anaerobiosis la típica reacción de color de C.
botulinum (esto es, una zona opaca alrededor de la colonia y una «capa
perlacia» en la superficie).

Las
colonias sospechosas se siembran después en caldo de carne cocida y en el
líquido sobrenadante se investiga la presencia de toxina botulínica después de
un tiempo de incubación suficiente. (el ensayo de la toxina se realiza a
veces en caldo de carne inoculado directamente con muestras del alimento
sospechoso). Finalmente en los extractos del alimento original puede intentarse
el ensayo directo de la toxina. En esencia los ensayos implican la inoculación de
los extractos del alimento o de los sobrenadantes de los cultivos a ratones, de
los que algunos se han protegido con antitoxinas A, B o E mientras que otros no
lo han sido. Los ratones inoculados se observan algunos días y si mueren los
que no se protegieron con las correspondientes antitoxinas con los signos
típicos de botulismo, mientras que viven los que lo fueron con la antitoxina
específica, la prueba es positiva al correspondiente tipo de C. botulinum. Antes
se han descrito los métodos de aislamiento de Clostridium botulinum, C.
perfringens y Bacillus cereus, pero puede necesitarse la enumeración del número
total de microorganismos esporulados del alimento. Como medida preliminar, las
muestras o diluciones que los contengan deberán calentarse a 80º C durante 10
minutos para destruir todas las células vegetativas, después se enfrían y
siembran. El calentamiento estimula la germinación de las esporas (choque
térmico), proceso que frecuentemente es difícil de iniciar sin un estímulo
adecuado. Para el recuento de Bacillus sp. se utilizan medios nutritivos
estándar, incubándose aeróbicamente. Obviamente los miembros de este grupo que
se encuentran en forma vegetativa en los alimentos, no se incluyen en el
recuento.

Para
los clostridios se necesita incubar en jarras cerradas cuyo aire es sustituido
por hidrógeno. los clostridios anaerobios obligados requieren la inclusión en
la jarra de un catalizador, como el paladio que convierte el oxígeno residual
en agua, al combinarse con el hidrógeno. A veces se realiza
un pre-enriquecimiento preliminar de la muestra, diluida en un medio de carne
cocida, sin embargo, para verificar el recuento, es preferible la siembra
directa en un medio sólido, nutritivamente complejo. Generalmente se emplea el
medio diferencial reforzado para clostridios (Differential Reinforced
Clostridial medium) de Gibbs y Freame (1965), que aunque líquido presenta
muchas ventajas. los recuentos son mayores que en medios sólidos y no se
requieren jarras anaeróbicas.
No
pueden hacerse recuentos exactos pero si se inoculan diluciones decimales se
obtienen cifras que se encuentran en un rango de valores que difieren en un
factor de diez (por ej., > 1.000 pero <10.000 por g). El medio contiene
un sistema indicador a base de una fuente de azufre y una sal de hierro, de
forma que el obscurecimiento del medio indica que han crecido clostridios la
mayoría de los cuales producen ácido sulfhídrico. Las colonias de Clostridios
sulfito reductores aparecerán de color negro debido a la formación de sulfuro
ferroso por reducción del sulfito. Transcurridas 48 h, contar el número de
colonias negras desarrolladas en la totalidad de la columna de agar, sin tener
en cuenta las puntiformes. El
resultado se expresará como número de esporas de clostridios sulfito reductores
en el volúmen de agua sembrado (20 ml a 100ml). Con objeto de evitar la
dificultad de recuento que puede producirse al confluir las colonias
desarrolladas se efectuará una primera lectura a las 24 h, y si por este motivo
no es posible el recuento a las 48 h se dará la lectura de las 24 h como
resultado aproximado.

El grupo bacteriano de los sulfito – reductores está integrado por microorganismos pertenecientes al género Clostridium y que tienen en común reducir el sulfito a sulfuro. Son muy resistentes por su capacidad de esporular. Se suelen usar para apreciar la calidad higiénica del agua y productos animales. Su número es escaso en productos frescos. La capacidad de esporular de estos microorganismos les confiere una gran resistencia. La detección de Clostridium sulfito – reductores se logra utilizando medios de cultivo en cuya fórmula interviene el sulfito de sodio, como el medio SPS, en los que, por la capacidad de estos microorganismos de reducir tal sustancia, se produce sulfuro de hierro al actuar sobre el compuesto de hierro. La presencia de sulfuro de hierro se pone de manifiesto por la aparición del color negro de las colonias.
El grupo bacteriano de los sulfito – reductores está integrado por microorganismos pertenecientes al género Clostridium y que tienen en común reducir el sulfito a sulfuro. Son muy resistentes por su capacidad de esporular. Se suelen usar para apreciar la calidad higiénica del agua y productos animales. Su número es escaso en productos frescos. La capacidad de esporular de estos microorganismos les confiere una gran resistencia. La detección de Clostridium sulfito – reductores se logra utilizando medios de cultivo en cuya fórmula interviene el sulfito de sodio, como el medio SPS, en los que, por la capacidad de estos microorganismos de reducir tal sustancia, se produce sulfuro de hierro al actuar sobre el compuesto de hierro. La presencia de sulfuro de hierro se pone de manifiesto por la aparición del color negro de las colonias.
Las pruebas bioquímicas consisten en distintos tests químicos aplicados a
medios biológicos, los cuales, conocida su reacción, nos permiten identificar
distintos microorganismos presentes, o sea, le damos su filiación, nombre y
apellido, al microorganismo investigado. Su sistema de funcionamiento generalmente consiste en determinar la
actividad de una vía metabólica a partir de un sustrato que se
incorpora en un medio de cultivo y que la bacteria al crecer incorpora o
no. Para realizar las pruebas bioquímicas se dispone
de múltiples medios, los cuales se deben aplicar de acuerdo a las
exigencias del microorganismo en estudio. De la amplia variedad de pruebas
bioquímicas, estudiaremos los resultados que estos test arrojan.
Objetivos
· Realizar el experimento adecuadamente
y poder identificar (aplicando éste método) a los distintos microorganismos, a
los cuales podremos darles “nombre y apellido”.
· Debemos conocer cuáles de los
test que componen las pruebas bioquímicas son los adecuados de acuerdo a la
circunstancia que necesitemos estudiar.
· Entender los principios bioquímicos de
las pruebas.
· Ser capaces de interpretar
adecuadamente los resultados entregados por las pruebas bioquímicas
· Conocer el uso de las pruebas
bioquímicas para la identificación de microorganismos
· Identificar errores de procedimiento en el laboratorio
al realizar los experimentos y poder reconocer en que partes del
procedimiento se cometió el o los errores, para así, mediante el desarrollo
experimental conocer más profundamente las pruebas bioquímicas.
PRUEBA DE LA OXIDASA
Pone de manifiesto la presencia de enzima oxidasa en ciertos
microorganismos. La oxidasa o citocromo oxidasa es una enzima que cede
electrones (H2), de un substrato al oxígeno, en el tren de transporte
electrónico. Pueden utilizarse diversos reactivos, que son colorantes que actúan como
aceptores de electrones, pasando en este caso de forma incolora o poco
coloreada, a fuertemente teñida. El reactivo más utilizado es el clorhidrato de
tetrametil-p – fenilendiamina al 1 por 100 en agua (Reactivo de Kovacs).
Existen comercializados discos o tiras de papel impregnadas de reactivos para
el diagnóstico de oxidasa. Se coloca un trozo de papel de filtro Whatman Nº 1,
dentro de una placa de Petri y se le añaden dos a tres gotas de reactivo. Con
un asa de platino (que no sea de hierro, ya que puede dar falsos positivos),
tomar una colonia de veinticuatro horas de desarrollo, y extenderla sobre el
papel de filtro mojado. La aparición de una coloración púrpura sobre la línea de inoculación se
considera como reacción positiva. Si no hay cambio de coloración, la prueba es
negativa.

PRUEBA DE LA CATALASA
La catalasa es una enzima propia de la mayoría de las bacterias aerobias y
anaerobias facultativas que poseen citocromos, con la excepción de Streptococcus. Su función es descomponer el
peróxido de hidrógeno (H202), desprendiendo oxígeno
libre. La prueba se puede realizar en porta o directamente sobre el cultivo. Se utiliza Agua oxigenada al 3 por 100 y se toma con el ansa una
colonia de 24 horas de desarrollo y se deposita sobre un porta. Añadir con una
pipeta una gota de agua oxigenada al 3 por 100; lo que no debe hacerse es
homogeneizar el asa con el cultivo sobre una gota de H202 depositada previamente en el porta,
pues produce falsos positivos. La prueba puede realizarse también añadiendo el agua oxigenada directamente
sobre una placa que contiene un cultivo puro. Si la colonia procede de una
placa de agar sangre puede dar falsos positivos debido a la presencia de
eritrocitos, que también poseen catalasa. Se considera la prueba positiva
cuando se observa desprendimiento de burbujas de gas (02).
PRUEBA DE ÓXIDO – FERMENTACIÓN (O – F) O DE HUGH LEIFSON
El medio de Hugh-Leifson es una base sin carbohidratos, a la que se puede
añadir después de esterilizarlo cualquier azúcar esterilizado previamente por
filtración. Cuando se habla de esta prueba sin especificar nada, hay que
suponer que el test se ha hecho con glucosa, así, cuando se dice que un
microorganismo es oxidante o fermentador se sobreentiende que lo es con
respecto al metabolismo de la glucosa. Esta prueba pone de manifiesto la propiedad que tienen determinados
microorganismos de actuar sobre los hidratos de carbono por vía oxidativa o
fermentativa. Las bacterias que no presentan actividad sobre los glúcidos, dan
esta prueba negativa. La prueba se realiza en dos tubos con medio semisólido y
rectos, que inicialmente son de color verde. Se inoculan por picadura en el
centro del tubo y uno de ellos se recubre con parafina líquida estéril (que
impide el contacto del medio con el oxígeno atmosférico).

El indicador en medio ácido (el metabolismo de los azúcares producen ácidos,
tanto en presencia como en ausencia de oxígeno) es de color amarillo. Si el
microorganismo es únicamente oxidante, después de la incubación sólo estará
amarillo el medio sin cubrir con parafina, si es oxidante y fermentador, en los
dos tubos el color vira a amarillo y si sólo puede utilizar el azúcar cuando
no hay oxígeno sería fermentador (tubo con parafina amarillo). El medio de
cultivo utilizado es el medio basal OF o de Hugh y Leifson. Inocular por picadura hasta 1/2 cm. del fondo del tubo. Para cada
microorganismo se siembran dos tubos, uno de los cuales contiene parafina.
Incubar a 37° C durante cuarenta y ocho horas o más. Los tubos se observan
diariamente hasta los catorce días. El viraje de color azul verdoso a amarillo,
indica que el microorganismo ha producido acidez a partir del azúcar. Si dicha coloración aparece solamente en el tubo que no está cubierto con
parafina, diremos que el microorganismo actúa sobre la glucosa (o el azúcar
utilizado) de forma oxidativa (O). Si se manifiesta en ambos, diremos que el
germen es fermentativo (F).

UTILIZACIÓN
DE LOS HIDRATOS DE CARBONO
Esta prueba determina la capacidad de un microorganismo para fermentar un
hidrato de carbono específico, incorporado a un medio de cultivo base,
produciendo ácido o ácido y gas. El indicador incluido en el medio es rojo de
fenol, que a pH 7,4 es de color rosa – rojizo y a pH ácido vira a amarillo. Los hidratos de carbono más utilizados son: glucosa, lactosa, sacarosa,
arabinosa, maltosa, manosa, rafinosa, fructosa, xilosa, trehalosa, galactosa,
ramnosa, melobiosa, almidón, manitol, sorbitol, inositol, adonitol, inulina,
salicina y amigdalina. Se prepara una solución al 10 por 100 del azúcar en agua
destilada y se esteriliza por filtración y el medio de cultivo es el Caldo base
púrpura de bromocresol. Una vez preparado el medio, se intuba a razón de 10 ml. en tubos que
contengan una campana de Durham. Añadir asépticamente la solución estéril de
carbohidrato para lograr una concentración final del 1 por ciento de azúcar.
Inocular una o dos colonias con el ansa de platino y la incubación en cada caso
se realiza a 37° C durante 24 – 48 horas.
La prueba nos permite observar:
· Producción de ácido: Medio de color
amarillo.
· No producción de ácido: Medio de
púrpura.
· Producción de gas (CO2 + H2): La presencia de aire
dentro de la campana de Durham indica que el microorganismo produce gas del
azúcar.
PRUEBA DE LA BETA-GALACTOSIDASA (ONPG)
Esta prueba demuestra la presencia de la enzima beta-galactosidasa en
algunos microorganismos. Hay bacterias que a pesar de poseer enzimas
hidrolizantes de la lactosa (beta - galactosidasas), no pueden actuar sobre
ella porque les faltan las enzimas extracelulares apropiadas (permeasas). A
estas bacterias se les denomina mutantes crípticos. Para conocer si un microorganismo es productor de betagalactosidasa, basta
añadir el compuesto orgánico: O – nitrofenil – beta – D – galactopiranósido
(ONPG) que es incoloro. Si la bacteria posee las enzimas hidrolizantes (beta –
galactosidasa), el compuesto se transforma en ortonitrofenol, un derivado
cromogénico de color amarillo. Todos los gérmenes denominados fermentadores
lentos de la lactosa son beta-galactosidasa positivos. Se utilizan discos
de ONPG, de los que se puede disponer comercializados. Preparar un inóculo muy
denso en 1 ml. de solución salina estéril, y añadir asépticamente un disco de
ONPG. Se favorece la reacción si la bacteria procede de un medio lactosado e
incubar a 37° C de veinte minutos a veinticuatro horas. Si el microorganismo es productor de beta-galactosidasa, el líquido se
volverá de color amarillo. Si queda incoloro, indicará que el microorganismo no
posee la enzima.

PRUEBA DE LA PRODUCCIÓN DE INDOL
La prueba del
indol determina la capacidad de las bacterias de degradar el triptófano dando
indol. Algunas bacterias, gracias a la enzima triptofanasa hidrolizan el
aminoácido, dando indol, ácido pirúvico y amoniaco. La presencia de indol se
detecta observando la formación de una coloración rosa – roja en el medio al
añadir para-dimetilaminobenzaldehído. Se utiliza un medio de cultivo rico en
triptófano, como el agua de peptona, o, mejor aún, el agua de triptona, pero
inmerso en una matriz semisólida como el Agar SIM (Indol, Movilidad y Sulfuro
de Hidrógeno), que nos permitirá la lectura de éstas tres pruebas simultáneas.
Se pueden utilizar dos reactivos:
1) Reactivo de Kovacs, y
2) Reactivo de Ehrlich.
En nuestra experiencia preferimos el primero, pero hay autores que
aconsejan el segundo, especialmente para determinados anaerobios.
a) Reactivo de Kovacs:
- Alcohol amílico o isoamílico: 150 ml.
- Para-dimetilaminobenzaldehído: 10 g.
- Acido clorhídrico concentrado: 50 ml.
Disolver el aldehído en el alcohol y agregar lentamente el ácido con
agitación constante. El reactivo es de color amarillo y se guarda protegido de
la luz y a 4° C.
b) Reactivo de Ehrlich:
- Para-dimetilaminobenzaldehído: 2 g.
- Alcohol etílico de 95°: 190 ml.
- Ácido clorhídrico concentrado: 40 ml.
Se prepara y almacena de igual modo que el reactivo de Kovacs. Inocular una o dos colonias, con ansa de platino puntiforme, en el Agar SIM
e incubar 24 – 48 horas a 37° C. Después de la incubación, añadir 5 gotas del Reactivo de Kovacs agitando
suavemente. La aparición de un anillo de color rojo en la superficie del medio
indica producción de indol. Si no se forma el anillo rojo, se considera la
prueba negativa.

PRUEBA DE VOGES PROSKAUER Y ROJO DE METILO
Las Enterobacterias clínicamente
importantes son anaerobias facultativas, y como tales, fermentan los hidratos
de carbono. Se conocen dos sistemas de fermentación para las Enterobacterias:
- Fermentación Acido Mixta: Producen Ácidos, CO2 y H2 , produciendo un gran descenso
del pH.
- Fermentación Butilenglicolica: Producen menor cantidad de ácidos y
Butilenglicol (Acetilmetilcarbinol), el descenso de pH es mucho menos
importante.
Estas dos pruebas se suelen realizar al mismo tiempo y se se siembran
simultáneamente en un mismo tubo con Caldo de Clark Lubs o Caldo Rojo de Metilo
– Voges Proskauer (RMVP) que posteriormente se dividen en dos para realizar
independientemente las pruebas. También se suelen considerar complementarias,
así ambas pruebas no dan positivo a la vez.
VOGES PROSKAUER
Se basa en la capacidad que poseen determinados microorganismos de producir
acetil – metil – carbinol a partir de la degradación de la glucosa mediante la fermentación Butilenglicolica. En presencia de oxígeno y de una
solución de K(OH) al 40%, el acetil – metil – carbinol se convierte en
diacetilo, el cual, en contacto con alfa – naftol produce color rojo. Se utiliza el Medio de Clark-Lubs o Caldo glucosa fosfato que es un medio
comercializado como Caldo RMVP. Inocular con ansa de platino, 1 o 2 colonias en
el caldo e incubar 24 – 48 horas a 37° C. Existen microorganismos que precisan
de otra temperatura de incubación o de un tiempo más prolongado. de los resultados
Después de la incubación añadir al caldo de cultivo 0,6 ml. de la solución
de alfa – naftol, y a continuación 0,2 ml. de la solución de hidróxido potásico
agitando unos instantes para favorecer un mayor contacto del líquido con el
oxígeno del aire. La lectura se efectúa después de diez a quince minutos de
añadir los reactivos, considerando como prueba positiva la aparición de una
coloración roja.
ROJO DE METILO
Se funda en la capacidad que poseen algunos microorganismos de actuar sobre
la glucosa, y a través del ácido pirúvico producir una fermentación ácido
mixta, capaz de bajar el pH a una cifra igual o inferior a 4,4. Se utiliza el
medio de Clark-Lubs descrito en la prueba de Voges-Proskauer, y como reactivo
la Solución de rojo de metilo al 0,5 por 100 en alcohol de 60º. Inocular una
colonia, con ansa de platino, en el caldo e incubar un mínimo de 48 horas a 37º
C. Determinados microorganismos necesitan una incubación más prolongada. Después de la
incubación, añadir cinco gotas del reactivo al caldo de cultivo. Se considera
la prueba como positiva si aparece una coloración roja. Una coloración amarilla
la califica como negativa, y una coloración anaranjada indica que la prueba es
dudosa y que se deberá repetir.

PRUEBA DEL CITRATO
Determina la capacidad que poseen algunos microorganismos de utilizar como
única fuente de carbono el citrato, produciendo alcalinidad. El medio utilizado
es el agar citratado de Simmons. Se inocula en estría, en el pico de flauta,
empezando desde el fondo hasta la parte más alta e incubar a 37° C durante
veinticuatro a cuarenta y ocho horas.
Son dos los aspectos que confirman la positividad de la prueba:
a) La
observación de crecimiento sobre el pico de flauta.
b) La variación
de coloración de verde a azul, debido a la alcalinización del medio,
producida por la liberación de sodio del citrato utilizado,
sodio, que con las moléculas de agua presentes formará Na(OH).
PRUEBA DE LA UREA
Determina la capacidad de un organismo para desdoblar la urea, en amoniaco
y CO2, por acción de la enzima ureasa. La visualización del proceso
se fundamenta en que la alcalinización producida en el medio de cultivo se
detecta mediante un indicador de pH (rojo de fenol). Se utiliza una solución de
urea al 20 por 100. Pesar 20 g. de urea deshidratada y disolverlos en 100 ml.
de agua destilada. No debe calentarse la solución ya que la urea se
desnaturaliza por el calor. Esterilizar por filtración, o utilizar erlenmeyer y
agua destilada estériles. Como medio base se utiliza el Medio Urea de Christensen.
Efectuar un inóculo denso en la zona del pico de flauta e incubar a 37° C
durante veinticuatro a cuarenta y ocho horas. Se considera la prueba positiva si el medio adquiere una tonalidad rosada,
y negativa si mantiene su coloración inicial.

PRUEBA DE LA DNasa
Se basa en la capacidad que poseen ciertas bacterias para hidrolizar
enzimáticamente el ácido desoxirribonucleico, produciendo una mezcla de mono y
polinucleótidos. Se utiliza el Agar DNA y como reactivo, el Ácido Clorhídrico 1
N. Sembrar una colonia del germen a investigar sobre una
placa de Agar DNA, de forma que después de la incubación quede una estría
superficial o un botón de crecimiento denso. Incubar 24 horas a 37° C. Cubrir las placas con HCl 1N. En caso de que el germen sea productor de
DNasa, se observa una zona clara alrededor del crecimiento. En caso negativo,
el medio permanece opaco.
PRUEBA DE LAS DESCARBOXILASAS
Algunas bacterias poseen unas enzimas descarboxilasas específicas que son
capaces de atacar el grupo carboxilo de determinados aminoácidos, produciendo
anhídrido carbónico y una amina, o diamina. Así la lisina decarboxilasa (LDC)
produce, a partir de la L – lisina: cadaverina (una diamina) y CO2. La ornitina
decarboxilasa (ODC) por acción sobre su L – aminoácido específico da
putresceína (diamina) y CO2. El aminoácido L – arginina posee un sistema especial de transformación:
primero por acción de una decarboxilasa se transforma en un producto
intermedio, la agmatina, la cual, por una dihidrolasa pasa a putresceína y
urea. Si el microorganismo es productor de ureasa transformará a su vez la urea
en amoniaco y anhídrido carbónico. Se utiliza el universalmente conocido Medio
de Möeller, que puede utilizarse como base para incluir cada uno de los
aminoácidos. La inoculación se realiza con un inóculo liviano de veinticuatro horas de
crecimiento, se cubren los tubos con 2 ó 3 mI. de parafina estéril para evitar
que el pH varíe (incluso en el patrón) y se incuban a 37° C por hasta cuatro
días. Se considera el resultado positivo cuando se observa una coloración
púrpura turbia. Una coloración amarilla (debida a la actuación de la bacteria
sobre la glucosa dando ácido) indicará que la prueba es negativa.

PRUEBA DE LA LISINA – HIERRO
En el medio de cultivo (Agar Lisina Hierro), la peptona y el extracto de
levadura aportan los nutrientes para el desarrollo bacteriano. La glucosa es el
hidrato de carbono fermentable, y la lisina es el sustrato utilizado para
detectar la presencia de las enzimas decarboxilasa y deaminasa. El citrato de
hierro y amonio, y el tiosulfato de sodio, son los indicadores de la producción
de ácido sulfhídrico. El púrpura de bromocresol, es el indicador de pH, el cual
es de color amarillo a pH igual o menor a 5.2, y de color violeta a pH igual o
mayor a 6.8. Por decarboxilación de la lisina, se produce la amina cadaverina,
que alcaliniza el medio y esto produce el viraje del indicador al color
violeta. La decarboxilación de la lisina, tiene lugar en medio ácido, por lo
que es necesario que la glucosa sea previamente fermentada. Los microorganismos que no producen lisina decarboxilasa, pero que son
fermentadores de la glucosa, producen un viraje de la totalidad del medio de
cultivo al amarillo, pero a las 24 hs de incubación se observa el pico de color
violeta debido al consumo de las peptonas, y el fondo amarillo.
La producción de sulfuro de hidrógeno, se visualiza por el ennegrecimiento
del medio debido a la formación de sulfuro de hierro. Las cepas de los
géneros Proteus, Providencia y algunas cepas de Morganella, desaminan la
lisina, esto produce un ácido alfa-ceto-carbónico, el cual, con la sal de
hierro y bajo la influencia del oxígeno forma un color rojizo en la superficie
del medio.
Se siembra por punción profunda con aguja de inoculación, incubándose en
aerobiosis, durante 24 horas a 37 °C.
- Prueba Positiva: Pico violeta/fondo violeta.
- Prueba Negativa: Pico violeta/fondo amarillo.
- Pico rojizo / fondo amarillo. Esto sucede con cepas del género Proteus,
Providencia y alguna cepas de Morganella spp.
- Prueba positiva de producción de ácido sulfhídrico: Ennegrecimiento del
medio (especialmente en el límite del pico y fondo)
Microorganismos
|
Color en el pico de
flauta
|
Color en la base del
tubo
|
Ennegrecimiento del
medio
|
Proteus mirabilis ATCC
43071
|
Rojo
|
Amarillo
|
Negativo
|
Salmonella typhimurium
ATCC 14028
|
Púrpura
|
Púrpura
|
Positivo
|
Salmonella enteritidis
ATCC 13076
|
Púrpura
|
Púrpura
|
Positivo
|
Providencia spp.
|
Rojo
|
Amarillo
|
Negativo
|
Citrobacter freundii
|
Púrpura
|
Amarillo
|
Positivo
|
Morganella spp.*
|
Rojo
|
Amarillo
|
Negativo
|
Edwarsiella spp.
|
Púrpura
|
Púrpura
|
Positivo
|
Klebsiella pneumoniae
ATCC 700603
|
Púrpura
|
Púrpura
|
Negativo
|
Escherichia coli ATCC
25922
|
Púrpura
|
Púrpura
|
Negativo
|
*Algunas
especies de Morganella spp., pueden desaminar la lisina.
PRUEBA DE MANITOL y MOVILIDAD
Se utiliza un medio semisólido el Agar SIM para detectar la movilidad, la producción de ácido sulfhídrico o sulfuro de hidrógeno y el indol de las
bacterias. Este medio puede contener manitol como fuente de carbono. Si el
microorganismo es capaz de usar el manitol se produce una acidificación del
medio, lo que da lugar a un viraje del indicador de pH de rojo a amarillo. Inocular por picadura un tubo
de medio semisólido con cada uno de los distintos microorganismos aislados.
Incubar 24 horas a 37°C y observar la zona de crecimiento del microorganismo y
si ha habido cambio en la coloración del medio. El test de la movilidad
se hace mirando el desplazamiento del microorganismo. Si el crecimiento se
limita a la zona de la picadura,
el microorganismo no es móvil. Si
el crecimiento se produce por
todo el medio, el microorganismo es
móvil.
PRUEBA DE REDUCCIÓN DEL NITRATO
Algunos microorganismos utilizan el nitrato en una vía alternativa como
fuente de energía, reduciéndolo a nitrito o a nitrógeno libre. Esta propiedad
es una característica importante en la diferenciación de muchos grupos
bacterianos. La presencia de nitrito en el medio se demuestra añadiendo alfa –
naftilamina y ácido sulfanílico, con la formación de un compuesto rojo: el
parasulfobencenoazo – alfa – naftilamina. Utilizaremos el medio Manitol Movilidad, con los siguientes reactivos:
Reactivo A:
- Alfa-naftilamina:
5 g.
- Acido
acético 5N al 30 por 100: csp 1.000 ml
Reactivo B:
- Acido
sulfanílico: 8 g.
- Acido
acético 5N al 30 por 100: csp 1.000 ml
Mantener los reactivos A y B en frasco oscuro y en la heladera sin
congelar. Sembrar por picadura e incubar a 37° C durante 24 – 48 horas. Añadir 0,5 ml. de reactivo A y a continuación 0,5 ml. del reactivo B. La
aparición de un color rojo después de treinta segundos indica la presencia de
nitritos en el medio. La reducción de los nitratos puede dar otros productos
más reducidos como amoniaco, nitrógeno molecular, óxido nítrico, óxido nitroso
o hidroxilamina, dependiendo de la especie bacteriana, en tal caso, después de
la adición del reactivo, no se aprecia cambio de color en el medio. Para confirmar que el proceso es negativo es necesario añadir una pequeña
cantidad de polvo de zinc, el cual, en caso de que existan nitratos, los reducirá
a nitritos, volviendo el medio de color rojo, e indicando consecuentemente que
antes no se había producido la reacción. Si después de la adición del polvo de
zinc el color no vira a rojo, indica que ha habido reducción y que el producto
obtenido no ha sido el nitrito.

PRUEBAS CON AGAR TRIPLE AZÚCAR – HIERRO (Agar TSI)
Son medios utilizados preferentemente para la diferenciación de la familia Enterobacteriaceae.
En ellos se puede determinar las fermentaciones de los hidratos de carbono, la
producción de gas y de ácido sulfhídrico. El Agar TSI contiene tres azúcares: glucosa y sacarosa (10 por 100) y
lactosa (1 por 100). Con una aguja de
inoculación se toma una colonia aislada y se siembra por picadura hasta unos
0,6 cm. del fondo. Se retira la aguja siguiendo el mismo camino de entrada y,
sin volver a cargar el asa, se siembra en estría la superficie del pico de
flauta. Incubar a 37° C
durante veinticuatro horas. Es importante respetar estos tiempos de incubación, ya que lecturas de
menor o mayor incubación pueden dar resultados falsamente positivos o
negativos. Se tendrán en cuenta los siguientes aspectos:
a) Producción de ácido a partir de la glucosa: Se pone de manifiesto en la
parte inferior del medio al producirse un cambio de color debido al viraje del
indicador de pH que pasa de rojo-naranja a amarillo (ácido).
b) Producción de gas a partir de la glucosa: Los gases producidos son el CO2 y el H2, productos
terminales del metabolismo de la glucosa, que se aprecia por la aparición de
burbujas en la parte inferior del medio, por una producción de grietas en su
interior o incluso por una elevación del medio que se separa del fondo.
c) Producción de ácido a partir de la lactosa: Se aprecia por un cambio de color
de rojo a amarillo en la parte del pico de flauta del medio.
d) Producción de sulfhídrico: Se manifiesta por un ennegrecimiento del
medio en la línea de inoculación o sobre la capa superficial.
En cultivos de bacterias muy productoras de SH2 a veces llega a ennegrecer
todo el medio, ocultando la reacción ácida de la parte inferior del medio
(tubo), pero si se ha formado SH2 es que existe una condición ácida en esa zona
por lo que se considerará el resultado, de la producción de ácido a partir de la
glucosa, como positivo.
PRUEBA DE LA FENILALANINA
Esta prueba determina la capacidad de un organismo para desaminar el
aminoácido fenilalanina en ácido fenilpirúvico por su actividad enzimática de
fenilalanina desaminasa, con la consiguiente acidez resultante. Esta actividad
enzimática es característica de todas las especies del género Proteus y del grupo Providencia por lo que se usa para separar ambos
géneros de otras Enterobacterias. Se cultiva el microorganismo en Agar fenilalanina sembrando la superficie
del pico de flauta con abundante inóculo e incubando durante 16 horas.
Seguidamente se añade 0,2 ml de una solución de cloruro férrico al 10% de manera
que inunde todo el crecimiento. La presencia de ácido fenilpirúvico (prueba
positiva) se manifiesta por la aparición de un color característico verde
oscuro o verde-azulado. La fenilalanina es un aminoácido que por desaminación oxidativa forma un
cetoácido, el ácido fenilpirúvico. Sólo los géneros Proteus y Providencia poseen la fenilalanina desaminasa, lo
que permite diferenciarlas del resto de las Enterobacterias. La prueba de la
fenilalanina se basa en la detección del ácido fenilpirúvico luego del
desarrollo del germen en un medio que contiene fenilalanina. Para eso se agrega
cloruro férrico que forma un complejo de color verde con el ácido
fenilpirúvico. El medio de cultivo no puede contener extractos de carne o
peptonas por su contenido variable en fenilalanina.
API 20E y SIMILARES
La batería de pruebas API20E es un sistema de identificación rápida para
bacterias de la familia Enterobacteriaceae y otras bacterias Gram(-).
Básicamente consta de 23 tests bioquímicos estandarizados y miniaturizados y
una base de datos. Este sistema presenta las ventajas de ser rápido, eficaz y
de permitir realizar numerosas pruebas a la vez. Cada tira de API 20E contiene
20 microtubos o pocillos con distintos sustratos deshidratados. Cada tubo es
una prueba bioquímica. Los microtubos se inoculan con una suspensión de microorganismos, en agua o
solución salina, que rehidrata los medios. Las tiras se incuban a 37°C y por
efecto del metabolismo bacteriano se van a producir cambios de color
espontáneos o bien al añadir reactivos. La lectura de las reacciones se hace
mediante comparación con una tabla de lectura donde se indica si los
microorganismos deben considerarse positivos o negativos para cada reacción
según el color aparecido. Tomar una colonia bien aislada de cada microorganismo y resuspenderla
homogéneamente en 5 ml de solución salina (1% de ClNa) o 5 ml de agua estéril. Poner la tira en la cámara de incubación. Previamente poner agua en los
alvéolos de la cámara para proporcionar una atmósfera húmeda durante la
incubación. Cada pocillo tiene un tubo y una cúpula. Llenar el tubo y la cúpula
de los pocillos | CIT | , | VP |, | GEL | con la suspensión de bacterias.
Llenar los tubos, no la cúpula, de los demás pocillos. Llenar con parafina las
cúpulas de los pocillos ADH, LDC, ODC, URE, H2S para obtener anaerobiosis. Incubar a 37 °C durante 18 – 24 h. La lectura de los resultados se lleva a cabo por comparación de los colores
de cada pocillo con los de la tabla de lectura.

Del conjunto de reacciones y resultados se obtiene un perfil numérico. Los pocillos están separados en grupos de tres: en total tenemos 7 tripletes (el test número 21 corresponde al test de la oxidasa). A cada pocillo se le da el valor 0, 1, 2 o 4. Si la reacción es negativa se pone 0. Si la reacción es positiva se pone: 1 si es el primer pocillo de un triplete, 2 si es el segundo, 4 si es el tercero. Se suman los valores de cada triplete y se obtiene un código de 7 cifras. Con este código se busca en la tabla de identificación la especie de que se trata.

Del conjunto de reacciones y resultados se obtiene un perfil numérico. Los pocillos están separados en grupos de tres: en total tenemos 7 tripletes (el test número 21 corresponde al test de la oxidasa). A cada pocillo se le da el valor 0, 1, 2 o 4. Si la reacción es negativa se pone 0. Si la reacción es positiva se pone: 1 si es el primer pocillo de un triplete, 2 si es el segundo, 4 si es el tercero. Se suman los valores de cada triplete y se obtiene un código de 7 cifras. Con este código se busca en la tabla de identificación la especie de que se trata.
"SOMOS LO QUE HACEMOS REPETIDAMENTE. EXCELENCIA, POR LO TANTO, NO ES UN ACTO SINO UN HÁBITO"
ARISTOTELES
LEGALES: El autor no asume responsabilidad alguna por la descarga, copia, distribución, modificación o alteración de los contenidos publicados, sean propios del mismo o de terceros, los cuales pudieren estar protegidos por Copyright, Derechos de Propiedad Intelectual, Derechos de Autor, o relacionados. La Bibliografía del tema expuesto y el crédito fotográfico está en poder del Autor y no se publica dada su extensión, pero se enviará por mail al interesado que la solicitare debidamente fundamentada.



Comentarios
Publicar un comentario